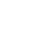外泌体研究
外泌体定量蛋白质组学服务
外泌体(Exosomes)是大小为30-150nm,具有磷脂双分子层膜结构的微小囊泡。外泌体可携带丰富的RNAs、脂质、蛋白质等生物活性分子,参与细胞间的通讯与调控。从外泌体研究专业数据库——ExoCarta和Vesiclepedia中记录的数据可以看出,外泌体携带的蛋白质的丰富程度尤为突出。外泌体蛋携带的蛋白质是外泌体标志物、外泌体载药、外泌体分子机制研究的主要分子抓手。
外泌体蛋白质也是登录CNS正刊最多的研究对象。除此之外,外泌体蛋白尤其是膜蛋白具有非常重要的临床转化价值,也是临床转化研究中的新宠。组织外泌体与血浆外泌体比对分析也成为发现新型疾病标志物的经典实验方案。

在外泌体蛋白标志物相关研究中,血浆/血清样本是主要研究载体。然而,血浆/血清中含有大量的载脂蛋白,如高密度脂蛋白质HDL,低密度脂蛋白质LDL,极低密度脂蛋白VLDL,乳糜微粒CM等。外泌体与这些脂蛋白质在物化性质上具有较大的相似性。常规的外泌体分离方法,如超速离心和沉淀法等都无法有效去除血浆/血清中的脂蛋白,严重干扰了下游质谱实验数据的检出率和可靠性。同时,实验样本来之不易,如何尽可能利用更少的样本获得更可靠的实验数据,成为外泌体蛋白质组学研究科研群体共同面对的技术问题。

| 外泌体蛋白质组服务
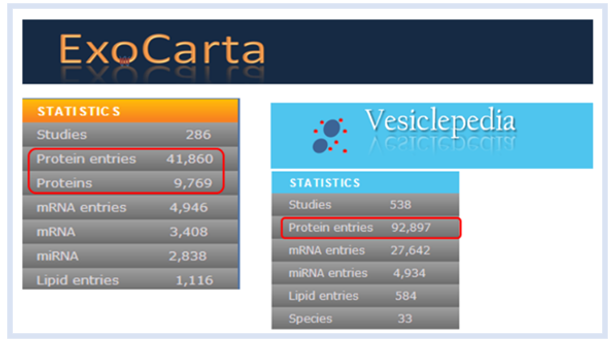
华盈生物开发了一套完整的外泌体蛋白质组学研究技术服务体系,针对不同类型的样本分别采用专属的外泌体提取方法,如超速离心、尺寸排阻、密度梯度离心等。同时,对蛋白质组学实验前处理进行了系统性创新优化,将样本用量降低的同时获取高质量数据,如利用0.5mL血浆即可完成外泌体的分离与蛋白质组筛选工作。
在样本使用量和检出蛋白数上,华盈生物的技术平台不断冲击外泌体蛋白质组学的检测的上限。例如:在人外泌体血浆蛋白组鉴定历史记录已达到2336种蛋白质,并且这个数据记录每天都可能被再次突破。截止目前,华盈生物已经完成超过30种样品类型的样品外泌体制备与分析。对于特殊样本如:胃液、脑积液、脑脊液、胆汁、微生物培养液、植物培养液等,也累积了丰富的项目经验,可承接复杂样品和项目的研究服务需求。
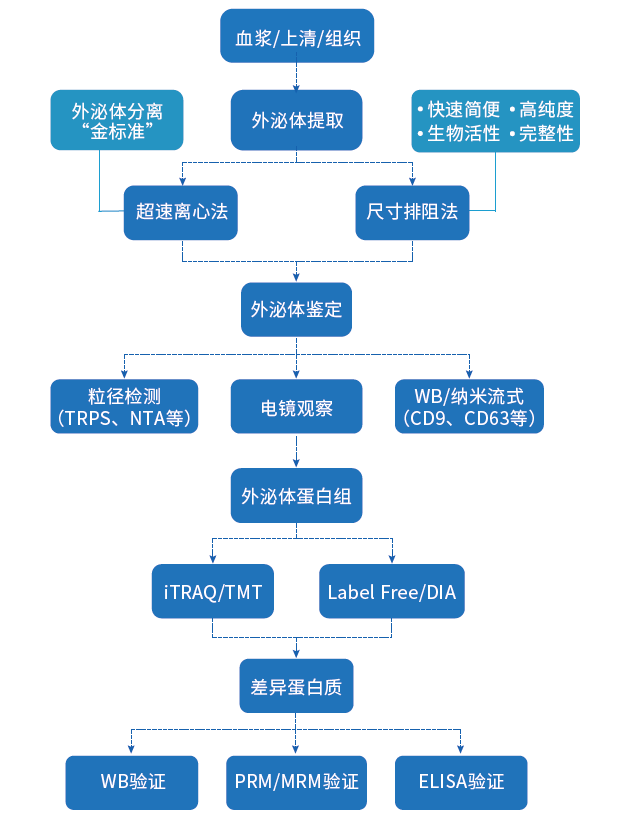
对于外泌体蛋白质组学研究来说,外泌体的纯度至关重要。在组织外泌体等热点研究领域,华盈生物经过系统的研发和比对分析,开发出的组织外泌体分离纯化方法可显著提高外泌体的纯度,达到Top杂志的要求。
华盈生物拥有质谱技术和抗体芯片两大平台,针对不同的研究需求,选择更优的技术。质谱技术对于鉴定能够在外泌体中携带的新蛋白(尤其是膜蛋白)具有显著优势,而抗体芯片则利用抗原抗体反应的特异性原理,对于外泌体中携带的分泌型的蛋白的鉴定更加灵敏和准确(抗体芯片目前可检测超过500种分泌蛋白)。
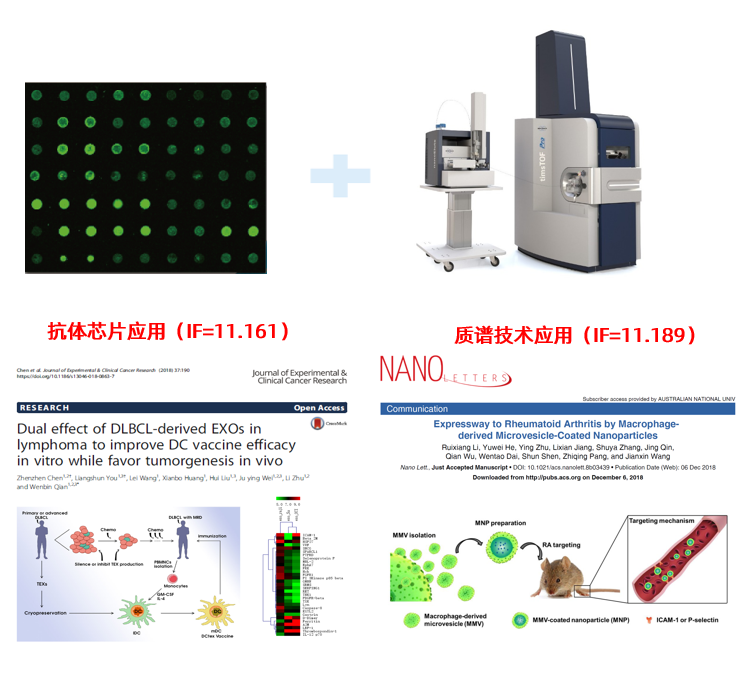
| 经典案例:血浆外泌体S100-A9蛋白激活NF-κB促进淋巴瘤复发
血浆中的外泌体蛋白既可以当作标志物,也可以进行机理研究?
首先,研究人员将慢性淋巴瘤(CLL)患者分为2个亚组:疾病进展期和疾病慢性期。然后利用质谱技术分析了患者血浆外泌体蛋白质组,发现S100-A9蛋白在进展期CLL患者中明显高表达,可以作为CLL进展期诊断的辅助标志物。进一步,研究人员通过生信分析发现进展期CLL患者外泌体中的高表达蛋白质主要与炎症和氧化应激有关,而NF-κB通路正是承接此效应的关键通路。通过从进展期CLL患者中分离富含S100-A9蛋白的外泌体加入CLL患者的PBMC细胞中,证实了S100-A9+外泌体能够明显促进进展期CLL患者PBMC细胞中IκBα蛋白的磷酸化上调,进一步激活NF-κB通路。
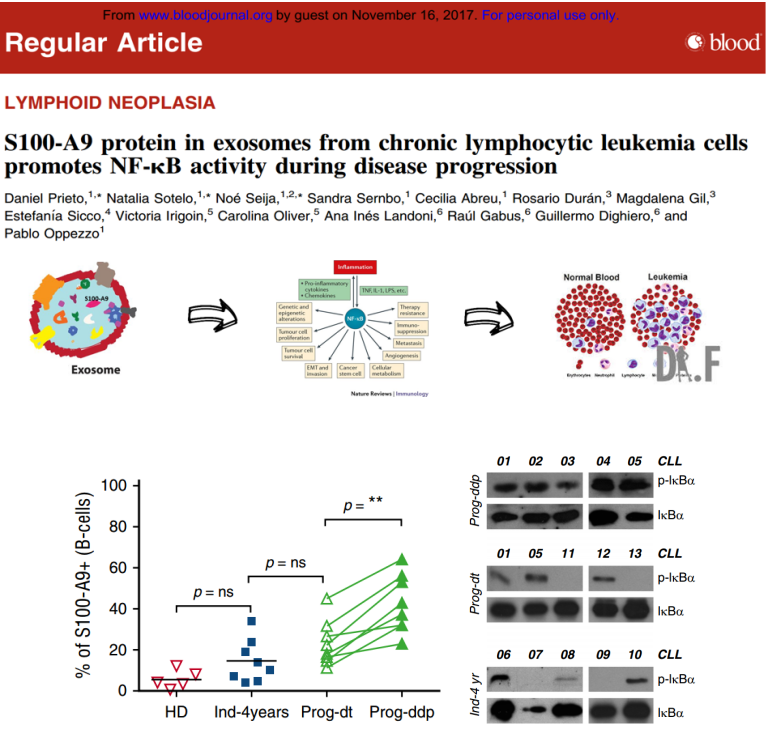
该研究证通过血浆外泌体蛋白组分析不仅找到辅助诊断进展期CLL的标志物,并证实了S100-A9+外泌体可通过形成正向反馈调控,不断激活进展期CLL患者自身PBMC细胞中的NF-κB通路,促进CLL进展的特殊机理。
| 客户文献
[1]. Chen, W. et al. Tumour‐associated macrophage‐derived DOCK7‐enriched extracellular vesicles drive tumour metastasis in colorectal cancer via the RAC1/ABCA1 axis. Clinical & Translational Med 14, e1591 (2024).(上海交通大学医学院附属上海总医院普外科 细胞上清) IF=10.4
[2]. Zhang, J. et al. Surface Engineering of HEK293 Cell-Derived Extracellular Vesicles for Improved Pharmacokinetic Profile and Targeted Delivery of IL-12 for the Treatment of Hepatocellular Carcinoma. IJN Volume 18, 209–223 (2023).(北京蛋白质组研究中心 细胞上清) IF=8.1
[3].Xiang, Z. et al. The diagnostic and prognostic value of serum exosome‐derived carbamoyl phosphate synthase 1 in HEV‐related acute liver failure patients. Journal of Medical Virology 94, 5015–5025 (2022)(南京医科大学 血清). IF=8.5
[4].Xu, M. et al. Stable expression of a truncated TLX variant drives differentiation of induced pluripotent stem cells into self-renewing neural stem cells for production of extracellular vesicles. Stem Cell Res Ther 13, 436 (2022).(北京蛋白质组研究中心 细胞上清) IF=8.0
[5].Luo, L. et al. Injectable cartilage matrix hydrogel loaded with cartilage endplate stem cells engineered to release exosomes for non-invasive treatment of intervertebral disc degeneration. Bioactive Materials 15, 29–43 (2022).(第三军医大学 细胞上清) IF=18.9
[6].Xia, C. et al. Autophagy and Exosome Coordinately Enhance Macrophage M1 Polarization and Recruitment in Influenza A Virus Infection. Front. Immunol. 13, 722053 (2022).(复旦大学药学院 细胞上清) IF=8.0
[7].Du, X. et al. Dynamic molecular choreography induced by traffic exposure: A randomized, crossover trial using multi-omics profiling. Journal of Hazardous Materials 424, 127359 (2022). (复旦大学公卫学院 血浆)IF=12.7
[8]. Zhang Luwen, Zhao Qiong, Cang Hui et al. Acute Myeloid Leukemia Cells Educate Mesenchymal Stromal Cells toward an Adipogenic Differentiation Propensity with Leukemia Promotion Capabilities. Adv Sci (Weinh), 2022, undefined: e2105811.(浙江大学医学院附属儿童医院 细胞上清)IF=15.1
[9]. Han Qiao, Jingtian Mei, Kai Yuan, et al. Immune-regulating strategy against rheumatoid arthritis by inducing tolerogenic dendritic cells with modified zinc peroxide nanoparticles. J Nanobiotechnology. 2022 Jul 14;20(1):323.(上海第九人民医院 细胞上清)IF=9.429
[10]. Qiao Yang, Mingjing Chen, Jiaoyang Gu, et al. Novel Biomarkers of Dynamic Blood PD-L1 Expression for Immune Checkpoint Inhibitors in Advanced Non-Small-Cell Lung Cancer Patients. Front Immunol. 2021 Apr 16;12:665133.(陆军军医大学新桥医院 血浆)IF=7.561
[11]. Tian Wang, Zhe Jian, Andrius Baskys, et al. MSC-derived exosomes protect against oxidative stress-induced skin injury via adaptive regulation of the NRF2 defense system. Biomaterials. 2020 Oct;257:120264.(西安市中心医院 细胞上清)IF=12.479
[12]. Ruixiang Li, Yuwei He, Ying Zhu, et al. Expressway to Rheumatoid Arthritis by Macrophage-derived Microvesicle-Coated Nanoparticles. Nano Lett. 2019 Jan 9;19(1):124-134.(复旦大学智能化递药教育部重点实验室 胶条)IF=10.8
[13]. Zhenzhen Chen, Liangshun You, Lei Wang, et al. Dual effect of DLBCL-derived EXOs in lymphoma to improve DC vaccine efficacy in vitro while favor tumorgenesis in vivo. J Exp Clin Cancer Res. 2018 Aug 13;37(1):190.(浙江大学医学院第一附属医院 细胞裂解液)IF=11.161

地址:上海市闵行区绿洲环路396弄5幢4层
电话:400-869-2936,021-33968791
邮箱:support@wayenbiotech.com
传真:021-33938792
QQ:2120485725
战略合作
战略合作
| Full Moon | RayBiotech | CDI | IZON | Bio-Rad | R&D Systems | IsoPlexis | Akoya | 南模生物 | 欧易生物 | 上海实验动物研究中心 | 美吉生物 | 麦特绘谱 |
特别说明:本网所有网页均为华盈生物原创信息,转载必须征求华盈生物同意,并同时注明本网名称及网址。
专利代码