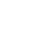信号通路是由从细胞膜、胞浆到细胞核一系列的蛋白分子,通过蛋白磷酸化和蛋白互作等形式串联起来的蛋白分子信号传导网络。在疾病的发生、发展,细胞表型等生物现象的背后,信号通路的调变起着分子层面的支撑作用。信号通路分析是肿瘤学、病理学、免疫学、细胞生物学、神经生物学、药理学等一系列以机理探索为研究目的的科研工作的必经之路。
然而,细胞中存在多条信号通路,它们并不孤立存在,会串联交叉形成的复杂信号网络(Cross-talk)。该信号网络在细胞受到胞外刺激后将信号通过级联放大、分散调节等方式传入胞内,引起一系列复杂的信号改变,进而产生综合的细胞应答。面对复杂研究现象,往往会有多条通路会发生调变。如何选择主要调变的通路?是困扰研究人员的主要难题之一,而传统的技术如Westen blot等不能解决。
升级版 信号通路广筛抗体芯片(CSP100 Plus)是在原肿瘤信号通路磷酸化广谱筛选抗体芯片(CSP100)的基础上升级完成的广筛芯片。该芯片采用三维高分子膜专用技术,在片基上共价结合304种高特异抗体,其中磷酸化抗体157种,非磷酸化抗体147种。一张CSP100 Plus芯片可以同时对16条信号通路进行筛选和比较。这16条信号通路是生物医学研究中常见也是重要的通路,它们广泛参与到肿瘤、免疫、心血管、神经系统、损失修复等多种病理生理过程中。因此,CSP100 Plus芯片可以适用于多种疾病与药物研究模型的信号通路筛选工作。同时,脊椎动物的磷酸化位点具备保守性,芯片上的抗体都是以目标蛋白的物种保守多肽序列为抗原进行设置,所以,CSP100 Plus芯片上的抗体具有一定的物种通用性。
| 抗体芯片特点
● 芯片规格为76 x 25 x 1 mm;
● 实现16条信号通路全面筛选;
● 每种抗体设置6次技术重复;
● 适用于组织、细胞等多类型样本;
● 5×106细胞、200 µg总蛋白量即可满足实验;
● 可同时提供磷酸化和蛋白表达两套数据;
● 可通用于人、小鼠、大鼠等多类型模式生物检测。
| 芯片覆盖通路
| 信号通路 |
蛋白数 |
|
PI3K-Akt signaling pathway
|
57
|
|
MAPK signaling pathway
|
49
|
|
Ras signaling pathway
|
40
|
|
ErbB signaling pathway
|
39
|
|
Focal adhesion
|
38
|
|
Apoptosis pathway
|
35
|
|
Insulin signaling pathway
|
32
|
|
Autophagy
|
29
|
|
mTOR signaling pathway
|
28
|
|
JAK-STAT signaling pathway
|
27
|
|
AMPK signaling pathway
|
25
|
|
Cell cycle
|
20
|
|
p53 signaling pathway
|
18
|
|
NF-kappa B signaling pathway
|
18
|
|
VEGF signaling pathway
|
17
|
|
TGF-beta signaling pathway
|
10
|
|
Others
|
13
|
点击下载检测列表
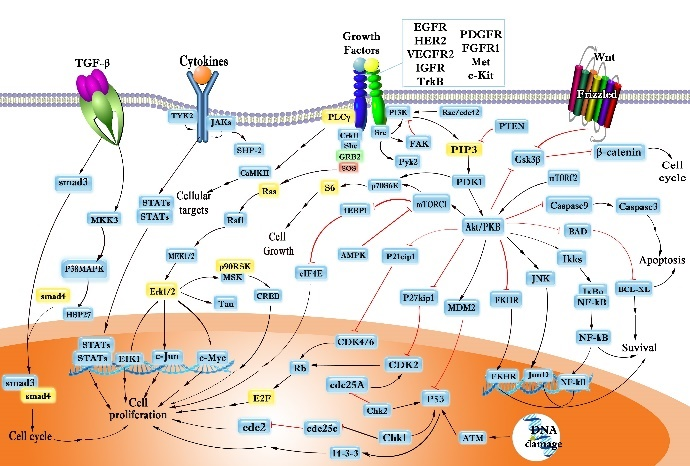
| 抗体芯片原理
| 客户案例:CSP100芯片协助发现纳米药物作用机理
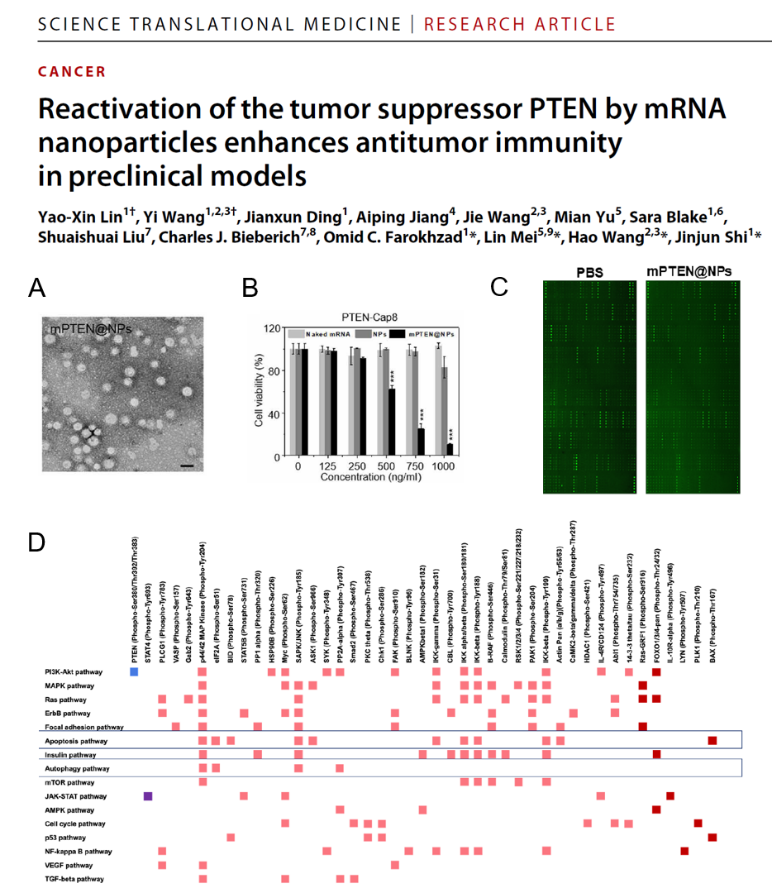
缺失和突变著名的抑癌基因PTEN 已经在很多癌症中被发现,由于PTEN可直接参与到抗肿瘤的免疫调节。因此,如果在癌症中重新开启PTEN基因的表达,通过增强抗肿瘤免疫,是否能够治疗肿瘤呢?这是一个非常有创意的假设。
研究人员通过PTEN mRNA 纳米颗粒(mPTEN@NP)载药系统(图1A)传递mRNA到基因缺失和突变的PTEN-Cap8 和B16F10 细胞中,恢复了PTEN基因的表达,果然达到了有效抑制前列腺癌细胞生长,促进其凋亡的疗效(图1B)。对于纳米药物领域的科学家来说,材料科学是本行,研究中纳米药物的改造往往会花费了大量精力。而对于PTEN这种明星分子的调控,又势必会引起一系列复杂信号通路的变化。如何高效地筛选这些信号通路成为需要面对的新问题?
研究人员与华盈生物展开紧密合作,通过CSP100信号通路磷酸化广筛抗体芯片技术,同时对mPTEN@NPs和PBS对照组分别处理的PTEN-Cap8细胞中的16条信号通路进行了广泛筛选(图1C)。芯片结果显示多条信号通路均围绕PTEN基因的表达发生了显著变化,尤其是自噬通路相关蛋白磷酸化调变尤为明显(图1D)。通过Western blot实验,研究人员证实了mPTEN@NP可显著增加自噬相关蛋白的表达。并通过一系列自噬相关功能实验,明确了自噬通过诱导损伤模式识别分子 (DAMPs),继而增加免疫原性细胞死亡(ICD)是mPTEN@NP发挥抗肿瘤作用的关键机制。
详细内容点击查看:https://mp.weixin.qq.com/s/dLS0iwFaUETn242avG2_lQ
| 客户文献
[1]. Bing Yao, Sha Zhu, Xiyi Wei, et al. The circSPON2/miR-331-3p axis regulates PRMT5, an epigenetic regulator of CAMK2N1 transcription and prostate cancer progression.Mol Cancer. 2022 May 27;21(1):119. (南方医科大学第一附属医院)IF=27.401
[2]. Chen C, Ma Q, Deng P, et al. 1800 MHz Radiofrequency Electromagnetic Field Impairs Neurite Outgrowth Through Inhibiting EPHA5 Signaling. Front Cell Dev Biol. 2021 Apr 12;9:657623.(第三军医大学)IF=6.684
[3]. Liu L, Wang Y, Geng C, et al. CD155 Promotes the Progression of Cervical Cancer Cells Through AKT/mTOR and NF-κB Pathways. Front Oncol. 2021 Jun 7;11:655302. (山东大学齐鲁医学院齐鲁医院)
[4]. Zhou Y, Fu B, Xu X, et al. PBX1 expression in uterine natural killer cells drives fetal growth. Sci Transl Med. 2020 Apr 1;12(537): eaax1798. (中科院先天免疫与慢性病重点实验室)IF=17.1
[5]. Zhou XX, Wang RL, Xue B, et al. Splicing factor SRSF1 promotes gliomagenesis via oncogenic splice-switching of MYO1B. J. Clin. Invest. 2019, 129: 676-693. (天津医科大学总医院)IF=14.808
[6]. Gu CM, Liu YJ, Yin Z, et al. Discovery of the Oncogenic Parp1, a Target of bcr-abl and a Potential Therapeutic, in mir-181a/PPFIA1 Signaling Pathway. Mol Ther Nucleic Acids. 2019 Jun 7;16:1-14. (暨南大学医学院中西医结合研究所)IF=8.8
[7]. Liu D, Zhang XX, Li MC, et al. C/EBPβ enhances platinum resistance of ovarian cancer cells by reprogramming H3K79 methylation. Nat Commun. 2018 Apr 30;9(1):1739. (武汉同济医院)IF=14.919
[8]. Ge XW, Chen JF, Li L, et al. Midostaurin potentiates rituximab antitumor activity in Burkitt’s lymphomaby inducing apoptosis. Cell Death Dis. 2018 Dec 18;10(1):8. (复旦大学中山医院病理科)IF=8.469
[9]. Wu QY, Zhu YY, Liu Y, et al. CUEDC2, a novel interacting partner of the SOCS1 protein, plays important roles in the leukaemogenesis of acute myeloid leukaemia. Cell Death Dis. 2018 Jul 10;9(7):774. (徐州医科大学附属医院)IF=9.0
[10]. Xu YZ, Dong BJ, Wang JF, et al. Sphingosine kinase 1 overexpression contributes to sunitinib resistance in clear cell renal cell carcinoma. Oncoimmunology. 2018 Sep 25;7(12):e1502130.(上海交通大学医学院仁济医院)IF=8.110
[11]. Du F, Sun LN, Chu Y, et al. DDIT4 promotes gastric cancer proliferation and tumorigenesis through the p53 and MAPK pathways. Cancer Commun (Lond). 2018 Jul 5;38(1):45. (第四军医大学肿瘤生物学国家重点实验室)IF=10.392
[12]. Ling SB, Xie HY, Yang F, et al. Metformin potentiates the effect of arsenic trioxide suppressing intrahepatic cholangiocarcinoma: roles of p38 MAPK, ERK3, and mTORC1. J Hematol Oncol. 2017 Feb 28;10(1):59. (浙江大学第一附属医院)IF=17.388
[13]. Zhu RR, Wang QX, Zhu YJ, et al. pH sensitive nano layered double hydroxides reduce the hematotoxicity and enhance the anticancer efficacy of etoposide on non-small cell lung cancer. Acta Biomater. 2016 Jan;29:320-332. (同济医院)IF=9.7