药物分析
外泌体蛋白组助力微环境细胞重编程
间充质基质细胞(MSCs)是组成骨髓(BM)微环境的主要细胞类型之一,具有分化的多功能性,并参与并调控白血病生长和耐药性。最近有报道显示白血病患者来源的MSCs的基因型和表型会发生改变,表明MSCs可能会被重编程。
2022年3月,浙江大学医学院陈烨研究员课题组揭示了急性髓性白血病来源的间充质干细胞倾向于分化为脂肪细胞的机制,相关研究成果以“Acute MyeloidLeukemia Cells Educate Mesenchymal Stromal Cells toward an Adipogenic Differentiation Propensity with Leukemia Promotion Capabilities”为题发表在Adv Sci (IF=16.806)上。

研究人员首先用正常和AML衍生的培养基培养hMSCs细胞,油红染色发现AML衍生的培养基表现出增强MSCs的脂肪生成和延迟的成骨分化能力(图1A)。随后AML细胞与hMSCs共培养发现,AML细胞促进正常hMSCs分化成脂肪谱系并延缓成骨分化(图1B)。进一步RNA-seq 分析发现体外实验中与AML共培养的MSCs中基因表达发生显著变化,主要富集在糖代谢等细胞过程上(图1C),并通过进一步确认了MSC的糖代谢上调(图1D)。
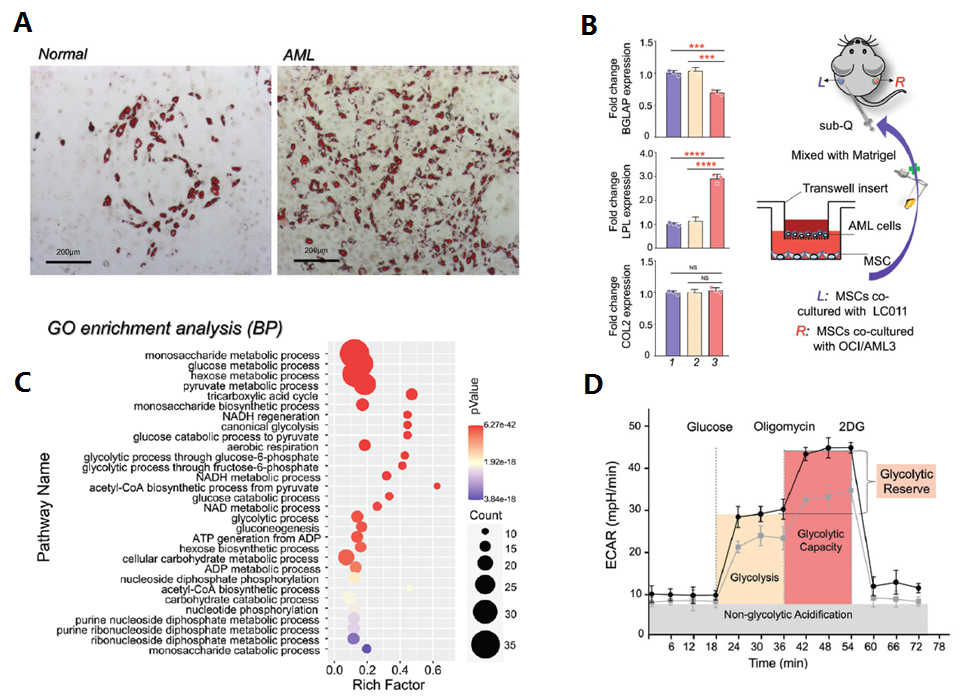
图1 AML细胞与hMSCs共培养促进hMSCs分化为脂肪细胞上调其糖代谢
外泌体因其在细胞间的通讯作用被广泛认知,为进一步解释AML细胞如何影响MSCs的行为,研究人员推测AML细胞可能是通过外泌体影响MSCs的。细胞共培养实验发现,AML细胞分泌的外泌体能够被hMSC摄取(图2A)并增强MSCs的脂肪生成和延迟的成骨分化能力(图2B)。通过TMT定量蛋白质组学分析(华盈生物提供技术服务),研究人员在AML分泌的外泌体中共鉴定了710种蛋白。这些蛋白主要与RNA转录(图2C)、糖代谢(图2D)等功能密切相关。外泌体定量蛋白组数据与RNA-seq指向一致,都说明与AML共培养的MSCs中糖代谢发生显著变化。最终通过深入研究表明,AML细胞可通过分泌富含糖代谢相关蛋白的外泌体间接调控MSCs细胞的糖代谢,进而引起MSCs细胞重编程的发生。
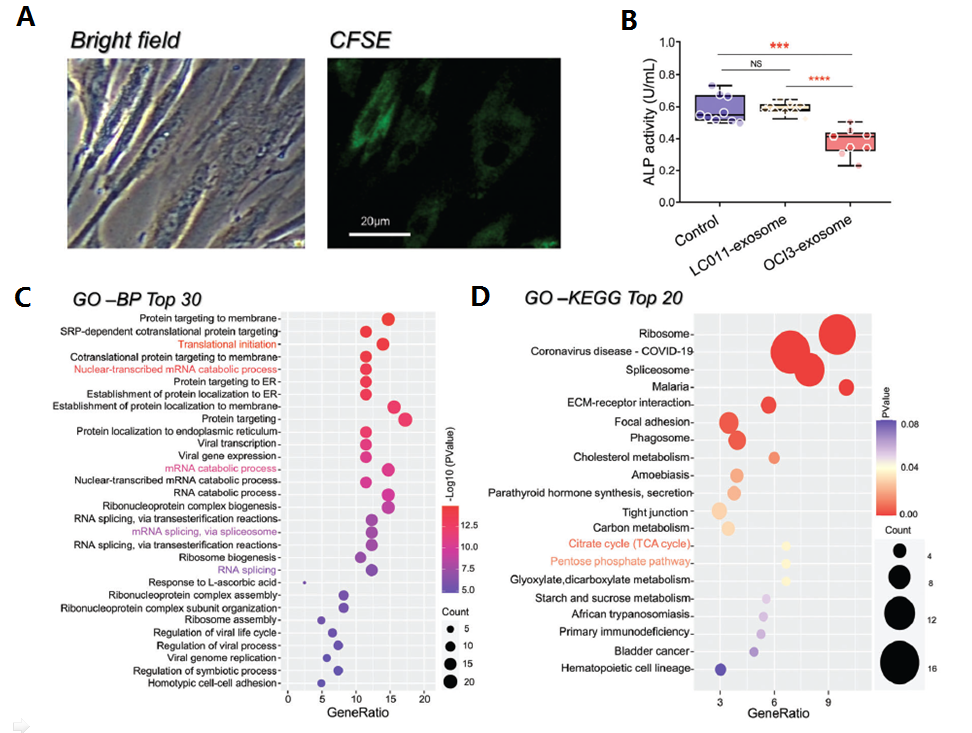
图2 AML细胞分泌的外泌体被hMSCs摄取影响其糖代谢
最后,为验证MSCs细胞重编程带来的体内影响,研究人员经过尾静脉注射AML衍生的外泌体到白血病小鼠体内,发现小鼠存活率显著降低,白血病表型更加明显(图3A-3C)。综上,该研究显示AML分泌的外泌体中的蛋白质使得MSCs倾向于分化成导致疾病进展的脂肪细胞,表明了白血病与微环境之间存在复杂的相互作用。同时,该研究中发现的外泌体蛋白及调控机制也为学界探索新的治疗AML的手段提供了科学基础。
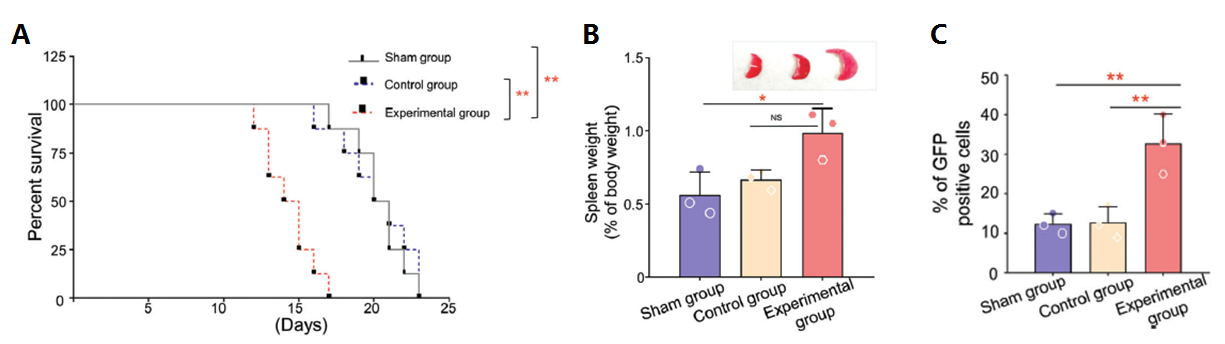
图3 AML细胞分泌的外泌体体内促进白血病发生
文献原文: Zhang L, Zhao Q, Cang H, et al. Acute Myeloid Leukemia Cells Educate Mesenchymal Stromal Cells toward an Adipogenic Differentiation Propensity with Leukemia Promotion Capabilities. Adv Sci (Weinh). 2022 Mar 20:e2105811.

地址:上海市闵行区绿洲环路396弄5幢4层
电话:400-869-2936,021-33968791
邮箱:support@wayenbiotech.com
传真:021-33938792
QQ:2120485725
战略合作
战略合作
| Full Moon | RayBiotech | CDI | IZON | Bio-Rad | R&D Systems | IsoPlexis | Akoya | 南模生物 | 欧易生物 | 上海实验动物研究中心 | 美吉生物 | 麦特绘谱 |
特别说明:本网所有网页均为华盈生物原创信息,转载必须征求华盈生物同意,并同时注明本网名称及网址。
专利代码