新闻资讯
高分文章策略三 “玩转”细胞因子—疾病标志物
- 分类:华盈视角
- 作者:华盈生物
- 来源:
【概要描述】细胞因子包括白介素,干扰素,肿瘤坏死因子和趋化因子等,可以通过多种生化途径和相互作用在体内发挥着促炎和抗炎的关键作用。
高分文章策略三 “玩转”细胞因子—疾病标志物
【概要描述】细胞因子包括白介素,干扰素,肿瘤坏死因子和趋化因子等,可以通过多种生化途径和相互作用在体内发挥着促炎和抗炎的关键作用。
- 分类:华盈视角
- 作者:华盈生物
- 来源:
- 发布时间:2022-05-23 10:28
- 访问量:
细胞因子包括白介素,干扰素,肿瘤坏死因子和趋化因子等,可以通过多种生化途径和相互作用在体内发挥着促炎和抗炎的关键作用。与其他类型的感染和炎性疾病测试方法相比,细胞因子的检测具有无创性和低成本的优势,已经作为诊断多种疾病的炎症标志物。今天华盈视角就为大家分享几篇细胞因子标志物研究的案例,领略细胞因子的独特魅力,一起学习细胞因子标志物的研究怎样设计和分析,最终揭示出最有价值的临床诊断指标。
| 案例一 血浆细胞因子预测黑色素瘤患者免疫治疗后的免疫相关不良事件
本研究在2019年发表于Clin Cancer Res杂志(IF:10.107)1。研究者利用抗体芯片技术对血浆65个细胞因子进行了检测。在发现阶段纳入了98个黑色素瘤病人,分为了两个组别:40个 anti-PD-1治疗患者,58个anti-PD-1联合anti-CTLA-4治疗患者(图1)。验证阶段纳入了49个anti-PD-1联合anti-CTLA-4治疗患者。研究者首先在发现阶段开展了纵向的比较研究,研究者收集了患者基线期(PRE),治疗早期(EDT)和中期(MID)的血浆,结果发现在这3个时期之间细胞因子并没有显著性的变化,说明了在免疫治疗进程中血浆细胞因子相对稳定。研究者然后在发现阶段对51个anti-PD-1联合anti-CTLA-4治疗患者进行了横向对比,其中有24个患者治疗后出现了严重的免疫相关不良事件(irAE)。细胞因子检测发现了在严重irAE患者基线期有17个上调的细胞因子,治疗早期有16个上调的细胞因子(FDR-adjusted P < 0.05; log2 FC > 0.7),其中11个在基线期和治疗早期都上调(图1)。最后研究者将这11个上调的细胞因子整合成了一个诊断指标值CYTOX score,ROC分析展示了CYTOX score在发现阶段和验证阶段都具有较高的诊断效能(图1)。
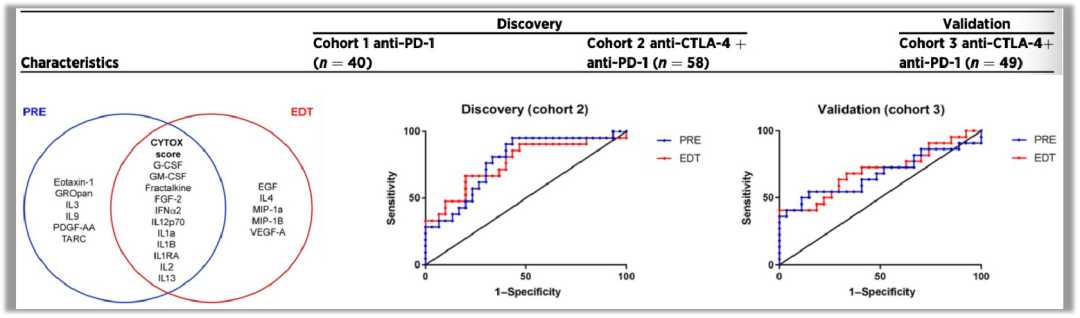
图1. 细胞因子预测黑色素瘤患者免疫治疗后的免疫相关不良事件。
ROC结果:cohort2, PRE: AUC=0.776; EDT: AUC=0.765; cohort3, PRE: AUC=0.675; EDT: AUC=0.
| 案例二 血浆和脑脊液中的细胞因子作为多发性硬化症的诊断标志物
本研究在2020年发表于Proc. Natl. Acad. Sci. U.S.A杂志(IF:9.412)2。本研究通过抗体芯片检测了脑脊液和血浆中的92个细胞因子。此研究在发现阶段纳入了136个多发性硬化症患者(MS),49个健康者(HC),35个其他神经疾病患者(OND)。验证阶段纳入了95个MS,47个HC,27个OND,86个症状相似的对照(SC)(图2A)。首先在发现阶段研究者对比了MS样本和其他样本,发现了11个显著性差异的脑脊液细胞因子(P < 5 × 10−5),其中有10个可以在验证阶段被成功验证出来(P < 0.05)(图2B)。在血浆样本中,研究者选取了发现阶段5个最显著差异的细胞因子在验证人群中验证,其中有2个细胞因子被成功验证(OSM,Pdis= 0.005, Prep= 2 × 10−4;HGF, Pdis= 0.01, Prep = 0.009)(图2B)。这些差异的细胞因子在发现阶段和验证阶段的相关性也都非常相似(图2B)。ROC分析展示了在发现人群和验证人群中脑脊液和血浆中的差异细胞因子单独,或者联合都可以高效的区分MS和其他疾病和健康者(图2C)。最后研究者也对其中药物治疗前后的MS患者进行了细胞因子检测,药物处理也会改变患者脑脊液和血液中的多种细胞因子(图2D,E),说明了细胞因子可以作为指示药效的标志物。
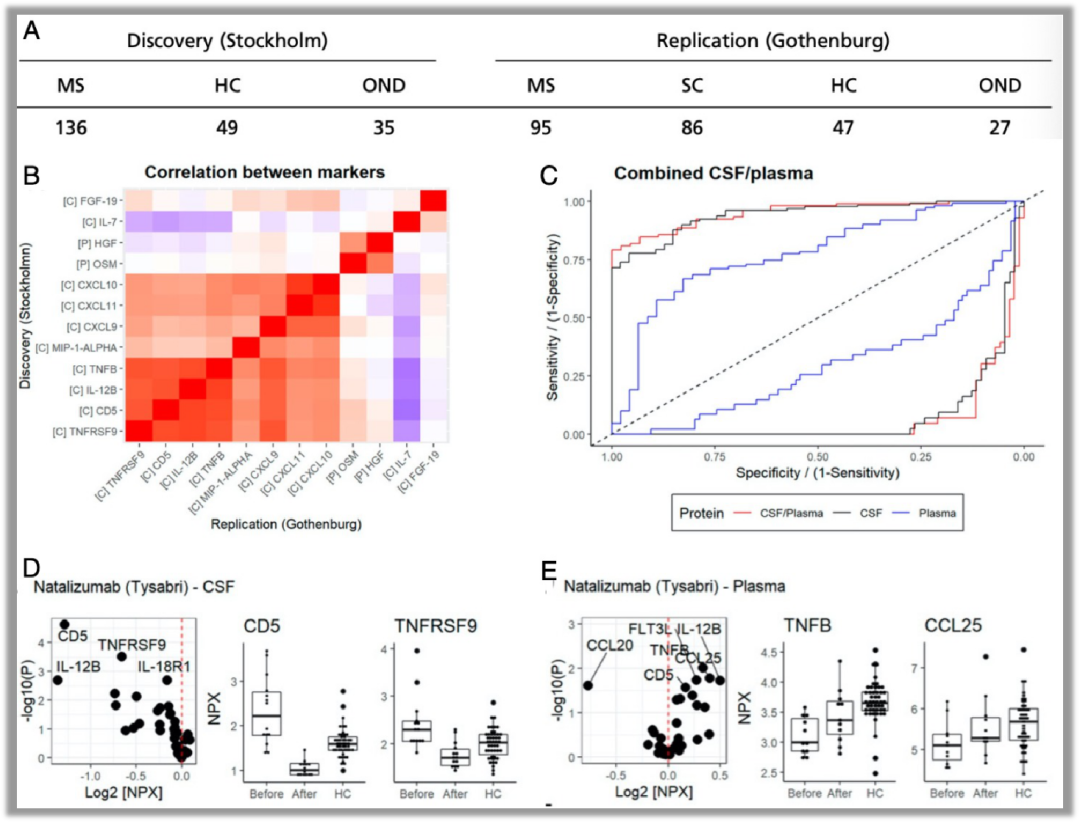
图2. 血浆和脑脊液中的细胞因子作为多发性硬化症的诊断标志物。
| 案例三 血清细胞因子预测白血病患者免疫治疗后的细胞因子释放综合症
此项研究在2016年发表于Cancer Discov杂志(IF:29.497)3。本研究通过Luminex检测了血清中44个细胞因子。研究者纳入了51个CTL019治疗的急性淋巴白血病患者,按照年龄分为了儿童组(n=39)和成年组(n=12)两个人群。研究者收集了基线期和治疗进程中不同时间点的血清进行细胞因子检测(图3A)。51个患者治疗后有48个患者出现了细胞因子释放综合症(CRS)(图3B)。研究者将CRS患者分为了严重性(n=14)和轻度性(n=34)。研究者对比了严重CRS和轻度CRS的所有样本检测结果,发现了24个细胞因子在严重CRS血清中显著上调。之后研究者通过机器学习建立了16个预测模型,ROC分析展示了在所有患者和不同年龄患者中不同组合形式的细胞因子都可以高效的区分严重CRS和轻度CRS(图3C,D)。
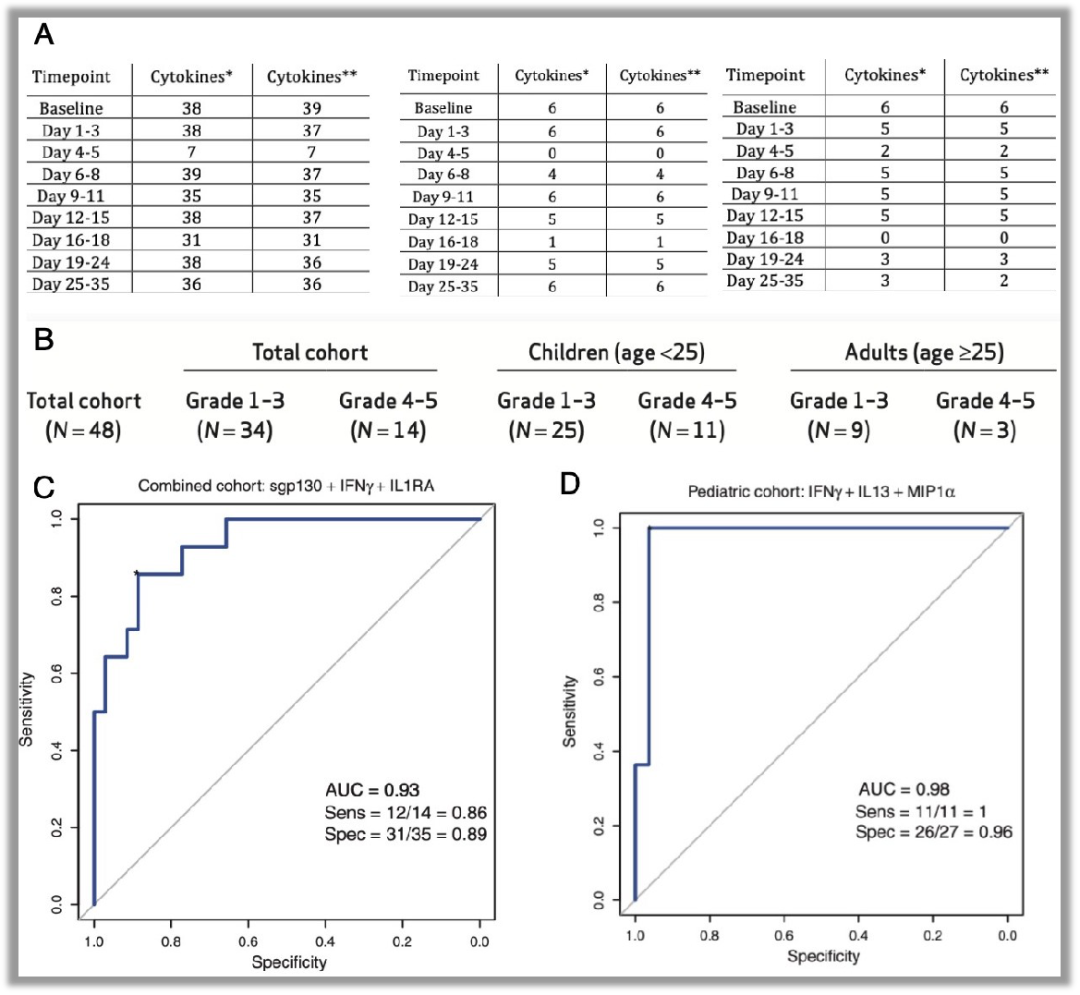
图3. 血清细胞因子预测白血病患者免疫治疗后的细胞因子释放综合症。
Timepoint: 血清收集的时间点;* 30-plex Luminex panel; ** 14-plex Luminex panel。数字代表患者数量,左表:儿童组;中间和右表:成年组。
| 案例四 肺泡灌洗液细胞因子+脂质组+基因表达联合诊断不同亚型的哮喘
本研究在2020年发表于J Allergy Clin Immunol杂志(IF:10.228)4。此项研究分析了肺泡灌洗液(BALF)中的3个指标:(1)通过Taqman分析了肺泡灌洗液细胞中32个免疫相关的基因和16个类二十烷酸途径的基因表达;(2)通过GC-MS分析了15个类二十烷酸分子;(3)通过Luminex分析了32个细胞因子。本研究纳入的病人包括22个患有非甾体类抗炎药加重呼吸系统疾病的哮喘病人(N-ERD),21个非甾体抗炎药耐受性哮喘患者(NTA)和11个健康对照者。研究首先根据哮喘患者BALF中免疫细胞的比例分为了4种亚型:嗜酸性细胞增多型(E),颗粒细胞缺乏型(P),中性粒细胞增多型(N),嗜酸性细胞和中性粒细胞增多型(E/N)。相比NTA组,N-ERD组中E型的比例更多(54.5% vs 9.5%)(图4A,B),嗜酸性细胞增多会上调TH2 细胞的基因表达,因此E型哮喘被称之为T2类型的哮喘。研究者然后对比了N-NED组中E型和non-E型肺泡灌洗液中的3个指标,发现E型N-NED中差异的基因,细胞因子和类二十烷酸都与嗜酸性细胞增多具有显著相关性,同时这3类指标间的也具有很高的相关性(图4C)。相比全身性的检测指标,肺泡灌洗液中的这些差异指标对于区分E型和non-E型N-NED更加准确(图4D)。最后研究者整合分析了所有哮喘患者的细胞因子和类二十烷酸检测指标,聚类分析形成了2个簇,分别是T2类型和non-T2类型(图4E)。与免疫细胞分型一致,根据这些差异指标,E型哮喘也都聚成一簇。同样这些差异指标可以高效的区分T2类型和non-T2类型哮喘(图4F)。
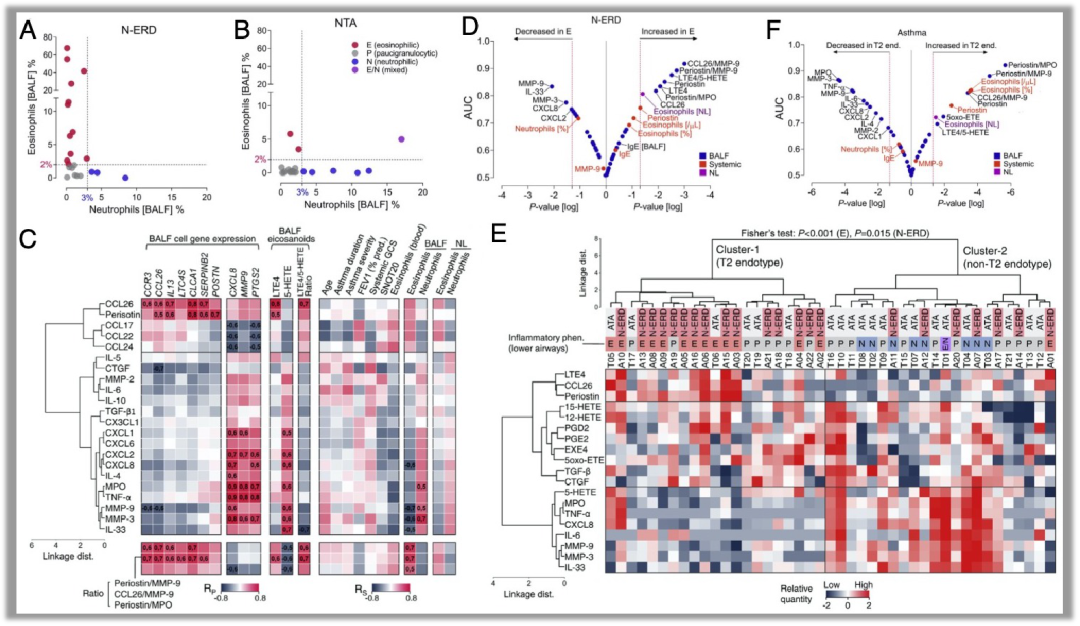
图4. 肺泡灌洗液细胞因子联合脂质组和基因表达诊断不同亚型的哮喘
| 案例五 血清细胞因子+蛋白质组联合诊断不同亚型的全身型幼年特发性关节炎
此研究在2019年发表于Ann Rheum Dis杂志(IF:16.102)5。本研究开展了血清label free蛋白质组和150个细胞因子的Luminex,及MRM-MS的血清标志物的筛选和验证研究。研究者总共纳入了136个病人,在发现阶段纳入了10个发热的全身型幼年特发性关节炎患者(SJIAsyst),10个多关节疾病的全身型幼年特发性关节炎患者(SJIApoly),10个患有关节疾病的感染病人(infection),在验证阶段纳入了45个SJIAsyst,29个SJIApoly,32个infection患者。研究者首先在发现阶段对比了SJIAsyst分别和SJIApoly,infection血清蛋白组,鉴别了总共72个差异蛋白,其中有48个蛋白可以在验证阶段通过MRM-MS分析,ROC分析了展示了30个最佳的多肽对应的蛋白可以非常高效的区分诊断SJIAsyst和SJIApoly(AUC=0.909)(图5A),以及SJIAsyst和infection(AUC=0.661)(图5A)。研究者在发现阶段对150个血清细胞因子进行筛选,去除无差异和检测不到的因子,最终研究者筛选出了17个细胞因子在验证阶段利用Luminex检测。最后研究者整合MRM和Luminex检测结果,ROC分析展示了血清蛋白组和细胞因子联合具有更高的诊断能力(SJIAsyst vs SJIApoly, AUC=0.918; SJIAsyst vs infection, AUC=0.803)(图5B)。另外分开比较MRM和Luminex检测的诊断效能,结果展示了Luminex检测的细胞因子比MRM鉴定的蛋白更能有效的区分诊断SJIAsyst和infection患者(AUC: 0.840 vs 0.661)(图5C),这不仅说明了对于诊断疾病的不同类型,蛋白质组和细胞因子具有各自的优势,还提示了同时检测多种类型的指标或者多组学联合分析的必要性。
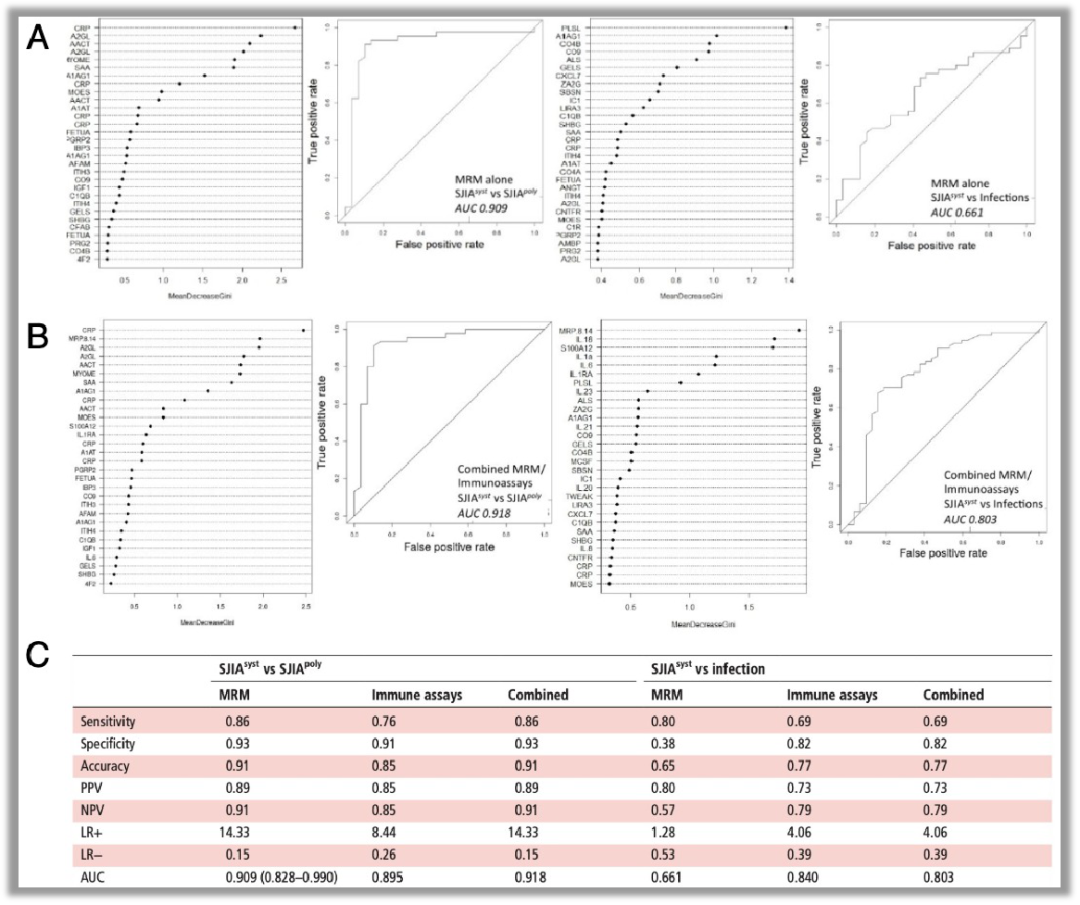
图5. 血清细胞因子+蛋白质组联合诊断不同亚型的全身型幼年特发性关节炎
从这几个精彩的案例可以看出细胞因子的检测毫无疑问具有很大的临床价值。那么怎样才能把细胞因子的价值体现出来呢,把这样的研究发到高分期刊上呢?上述的研究案例或许给出了一定的启示。首先这些案例的临床样本并不是很多,但是在样本分组设计上都非常的巧妙,病人分层的细化程度很高,同种疾病的亚型多样化;其次对病人治疗前后的纵向跟踪;然后就是细胞因子与其他检测指标联合分析,包括实验室指标,蛋白组学,脂质组,代谢组和转录组。如此的研究思路和策略定能助力大家的研究更易被高分期刊接收。
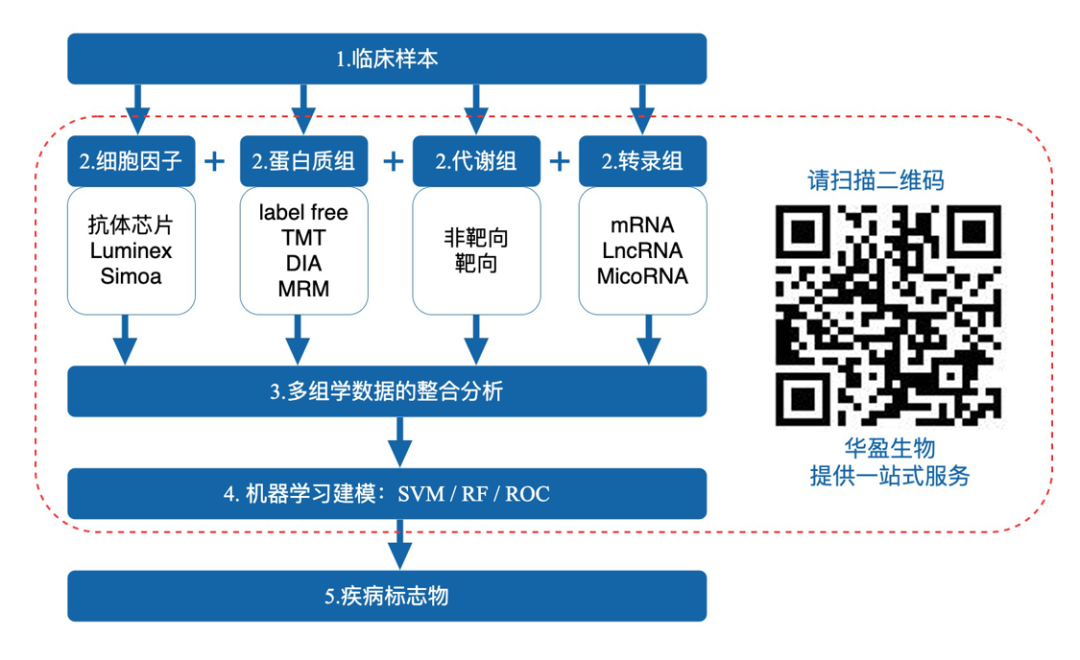
图6. 细胞因子标志物研究策略
除了以上研究方案上的创新,细胞因子的研究还存在检测方法灵敏度的问题。相当一部分因子在血浆/血清中含量很低,普通的ELISA很难检测到,例如神经相关的因子,还有像IL-2、IL-6、IL-17A、TNF-α等丰度极低的炎症因子等。例如第5个案例中研究者筛选150个细胞因子,发现部分因子无法检测到而剔除,那么引起了一个问题:这些无法检测因子与疾病也具有相关性,怎样才能检测到呢?近年来盛起的Simoa(Single-molecule Array)技术可谓一骑绝尘,灵敏度比ELISA提高出1000倍以上,它的出现将蛋白质检测技术直接带入到单分子、数字化检测时代,成为fg级超低丰度蛋白质检测领域的优势技术。David Yeung等6研究人员对比了目前世界上几乎所有超敏蛋白质检测技术对于IL-2、IL-6、IL-17A、TNF-α等低丰度炎症因子的检测情况,发现Simoa技术无论在灵敏度还是在数据重现性上,相比其他技术均具有显著优势。利用Simoa细胞因子 6‐plex Panel 可以检测到低至2 fg/ml的IL‐12p70(图7)。Simoa还可以在血清/血浆中检测NfL、Tau、pTau、Aβ40、Aβ42等超低丰度神经因子,例如在阿尔兹海默症初期(提前16年),Simoa可以在接近正常人的患者血清中检测到蛋白标志物NfL7。由此可见Simoa的检测能力真的超乎我们的想象,可以满足其它技术无法完成的检测需求。
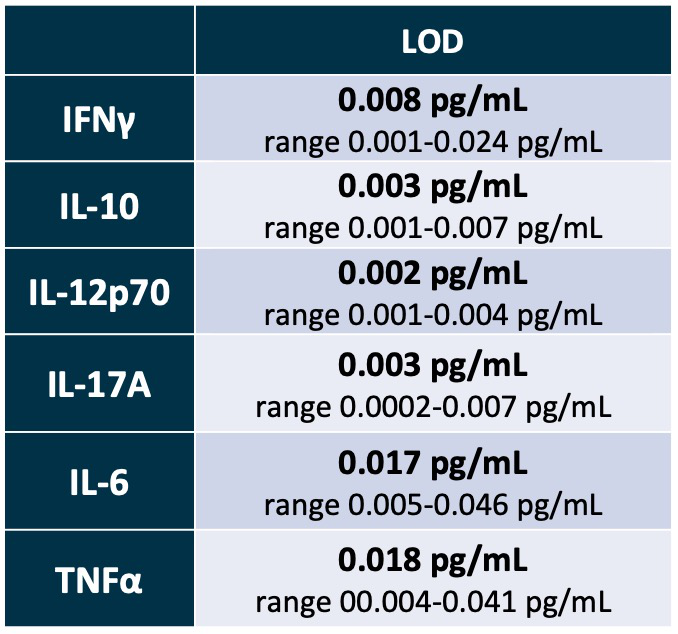
图7. Simoa细胞因子 6‐plex Panel检测因子的下限范围
LOD:Limit of Detection,详见https://www.quanterix.com/technology
华盈生物拥有“高通量抗体芯片”(解决标志物筛选阶段需求)、“Luminex液相悬浮芯片” (解决标志物验证阶段需求)、“单分子高敏Simoa技术” (解决超低丰度细胞因子检出需求)三个细胞因子检测平台,三平台各具优势,经过华盈生物有机组合,可满足细胞因子标志物全方位需。在蛋白标志物研究筛选、验证、转化的各环节,华盈生物均能够为科研人员提供适合的技术选择,帮助科研人员获得更高质量的科研数据。

图8. 华盈生物细胞因子检测“一站式”服务平台
| 相关文献
1. Lim SY, Lee JH, Gide TN et al., Circulating Cytokines Predict Immune-Related Toxicity in Melanoma Patients Receiving Anti-PD-1-Based Immunotherapy. [J]. Clin Cancer Res. 2019;25(5):1557-1563.
2. Huang J, Khademi M, Fugger L et al., Inflammation-related plasma and CSF biomarkers for multiple sclerosis. [J]. Proc Natl Acad Sci U S A. 2020;117(23):12952-12960.
3. Teachey DT, Lacey SF, Shaw PA et al., Identification of Predictive Biomarkers for Cytokine Release Syndrome after Chimeric Antigen Receptor T-cell Therapy for Acute Lymphoblastic Leukemia. [J]. Cancer Discov. 2016;6(6):664-679.
4. Jakiela B, Soja J, Sladek K et al., Heterogeneity of lower airway inflammation in patients with NSAID-exacerbated respiratory disease. [J]. J Allergy Clin Immunol. 2020;S0091-6749(20)31135-0.
5. Gohar F, McArdle A, Jones M et al., Molecular signature characterisation of different inflammatory phenotypes of systemic juvenile idiopathic arthritis. [J]. Ann Rheum Dis. 2019;78(8):1107-1113.
6. Yeung D, Ciotti S, Purushothama S et al., Evaluation of highly sensitive immunoassay technologies for quantitative measurements of sub-pg/mL levels of cytokines in human serum. [J]. J Immunol Methods. 2016;437:53-63.
7. Preische O, Schultz SA, Apel A et al., Serum neurofilament dynamics predicts neurodegeneration and clinical progression in presymptomatic Alzheimer's disease. [J]. Nat Med. 2019;25(2):277-283.

地址:上海市闵行区绿洲环路396弄5幢4层
电话:400-869-2936,021-33968791
邮箱:support@wayenbiotech.com
传真:021-33938792
QQ:2120485725
战略合作
战略合作
| Full Moon | RayBiotech | CDI | IZON | Bio-Rad | R&D Systems | IsoPlexis | Akoya | 南模生物 | 欧易生物 | 上海实验动物研究中心 | 美吉生物 | 麦特绘谱 |
特别说明:本网所有网页均为华盈生物原创信息,转载必须征求华盈生物同意,并同时注明本网名称及网址。
专利代码